Bikalutamidi
| |

| |
Bikalutamidi
| |
| Systemaattinen (IUPAC) nimi | |
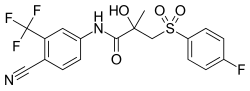
| N-[4-syano-3-(trifluorimetyyli)fenyyli]-3-(4-fluorifenyyli)sulfonyyli-2-hydroksi-2-metyylipropanamidi | |
| Tunnisteet | |
| CAS-numero | |
| ATC-koodi | L02 |
| PubChem CID | |
| DrugBank | |
| Kemialliset tiedot | |
| Kaava | C18H14N2F4O4S |
| Moolimassa | 430,382 |
| SMILES | Etsi tietokannasta: , |
| Fysikaaliset tiedot | |
| Sulamispiste | 191–193 °C [1] |
| Farmakokineettiset tiedot | |
| Hyötyosuus | ? |
| Proteiinisitoutuminen | 95 %[2] |
| Metabolia | Hepaattinen |
| Puoliintumisaika | n. 6 vrk |
| Ekskreetio | ? |
| Terapeuttiset näkökohdat | |
| Raskauskategoria |
? |
| Reseptiluokitus |
|
| Antotapa | Oraalinen |
Bikalutamidi (C18H14SN2O4F4) on orgaaninen yhdiste. Yhdistettä käytetään lääketieteessä eturauhassyövän hoidossa. Bikalutamidi kuuluu WHO:n ylläpitämälle listalle tärkeimmistä lääkeaineista[3].
Ominaisuudet
[muokkaa | muokkaa wikitekstiä]Bikalutamidin vaikutusmekanismi perustuu siihen, että se on androgeenireseptorien toiminnan estäjä. Tällöin androgeenihormonien, erityisesti testosteronin vaikutukset syöpäsoluissa eivät ilmene. Bikalutamidi on optisesti aktiivinen yhdiste, ja ainoastaan (R)-enantiomeerilla on lääkeaineena aktiivisuutta. (S)-enantiomeeri metaboloituu nopeasti ja on inaktiivinen. Bikalutamidia käytetään erityisesti etäpesäkkeitä muodostavan eturauhassyövän hoidossa. Sitä käytetään yhdessä leikkaushoidon, kastroinnin ja gonadoliberiinihormonin agonistin kanssa. Bikalutamidi sitoutuu androgeenireseptoreihin noin kaksi kertaa niin tehokkaasti kuin vanhemmat lääkeaineet flutamidi ja nilutamidi.[2][4][5][6]
Haittavaikutukset
[muokkaa | muokkaa wikitekstiä]Tyypillisin bikalutamidin aiheuttama haittavaikutus on kuumat aallot, joita ilmenee noin puolella potilaista. Lisäksi mahdollisia haittavaikutuksia ovat gynekomastia eli rintojen suurentuminen, allergiset oireet, erektiohäiriöt ja alentunut seksuaalinen halukkuus. Ruuansulatuskanavan oireet ovat harvinaisia, mutta mahdollisia.[2][6]
Synteesi
[muokkaa | muokkaa wikitekstiä]Bikalutamidin valmistuksen ensimmäisessä vaiheessa metyylimetakrylaatin kaksoissidos hapetetaan epoksidiksi vetyperoksidin avulla. Seuraavassa vaiheessa p-fluoritiofenoli reagoi tämän tuotteen kanssa, jolloin epoksidirengas aukeaa. Sitä seuraa esterin hydrolyysi, ja muodostunut karboksyylihappo reagoi 4-syano-3-trifluorimetyylianiliinin kanssa muodostaen amidin tionyylikloridin läsnä ollessa. Viimeisessä vaiheessa tuotteen tioeetteriryhmä hapetetaan sulfoniryhmäksi m-klooriperbentsoehapon avulla.[4]
Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ Susan Budavari (päätoim.): Merck Index, s. 201–202. (12th Edition) Merck & Co., 1996. ISBN 0911910-12-3 (englanniksi)
- ↑ a b c Michael Clinton Perry: The Chemotherapy Source Book, s. 579–580. Lippincott Williams & Wilkins, 2008. ISBN 978-0781773287 Kirja Googlen teoshaussa (viitattu 3.9.2017). (englanniksi)
- ↑ WHO Model List of Essential Medicines 2015. WHO. Viitattu 3.9.2017. (englanniksi)
- ↑ a b Axel Kleemann: Antineoplastic Agents, 2. Hormonally Acting, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2010. Viitattu 3.9.2017.
- ↑ David A. Williams, William O. Foye, Thomas L. Lemke: Foye's principles of medicinal chemistry, s. 1372. Lippincott Williams & Wilkins, 2012. ISBN 9781609133450 Kirja Googlen teoshaussa (viitattu 3.9.2017). (englanniksi)
- ↑ a b Georg F. Weber: Molecular Therapies of Cancer, s. 317–318. Springer, 2015. ISBN 978-3-319-13277-8 Kirja Googlen teoshaussa (viitattu 3.9.2017). (englanniksi)