Kaliumsuperoksidi
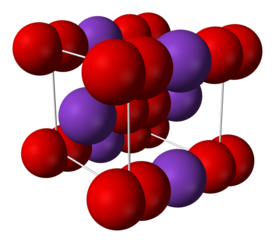
| Kaliumsuperoksidi | |
|---|---|
 |
|
| Tunnisteet | |
| CAS-numero | |
| PubChem CID | |
| Ominaisuudet | |
| Molekyylikaava | KO2 |
| Moolimassa | 71,1 |
| Ulkomuoto | Keltainen kiteinen aine |
| Sulamispiste | 380 °C[1] |
| Tiheys | 2,14 g/cm3[1] |
Kaliumsuperoksidi (KO2) on kalium- ja superoksidi-ioneista koostuva epäorgaaninen ioniyhdiste. Kaliumsuperoksidi on yksi kaliumin oksideista. Sitä käytetään hapen vapauttamiseen ja orgaanisessa synteesissä.
Ominaisuudet, valmistus ja käyttö
[muokkaa | muokkaa wikitekstiä]Kaliumsuperoksidi on huoneenlämpötilassa keltaista kiinteää ainetta. Yhdiste on voimakas hapetin ja reagoi veden kanssa muodostaen kaliumhydroksidia, vetyperoksidia ja happikaasua. Lisäksi kaliumsuperoksidi reagoi hiilidioksidin kanssa vapauttaen happea ja muodostaen kaliumkarbonaattia.[1][2][3]
- 2 KO2 + 2 H2O → 2 KOH + H2O2 + O2
- 4 KO2 + 2 CO2 → 2 K2CO3 + O2
Kaliumsuperoksidia muodostuu kuumennettaessa kaliummetallia happivirrassa.[1][2][3]
- K + O2 → KO2
Koska kaliumsuperoksidi vapauttaa happea kosteuden ja hiilidioksidin vaikutuksesta, sitä käytetään happinaamareissa sekä hapen tuottajana sukellusveneissä ja avaruussukkuloissa. Orgaanisessa synteesissä kaliumsuperoksidia voidaan käyttää ketonien valmistamiseen bentsyylisistä metyleeniyhdisteistä ja hydroksiketonien valmistamiseen ketoneista.[2][3]
Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ a b c d Thomas Scott, Mary Eagleson: Concise encyclopedia chemistry, s. 889. Walter de Gruyter, 1994. ISBN 978-3110114515 Kirja Googlen teoshaussa Viitattu 09.12.2012. (englanniksi)
- ↑ a b c Geoff Rayner-Canham & Tina Overton: Descriptive Inorganic Chemistry, s. 258. (5th Edition) W. H. Freeman and Company, 2006. ISBN 978-1-4292-2434-5 (englanniksi)
- ↑ a b c Kuen-Wai Chiu: Potassium, Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, New York, 2005. Viitattu 09.12.2012